ミトコンドリア病 治験レポート 第23号を配信中(2026.2.17)
・配信中の治験レポートでは現在募集中の治験についての詳しい情報を掲載しています(レポートのイメージはこちら)
・ミトコンドリア病と遺伝子検査について詳しくはこちら
治験に関する情報 対象疾患:ミトコンドリア病(指定難病21)
国内治験等一覧治験等の状況国外の候補
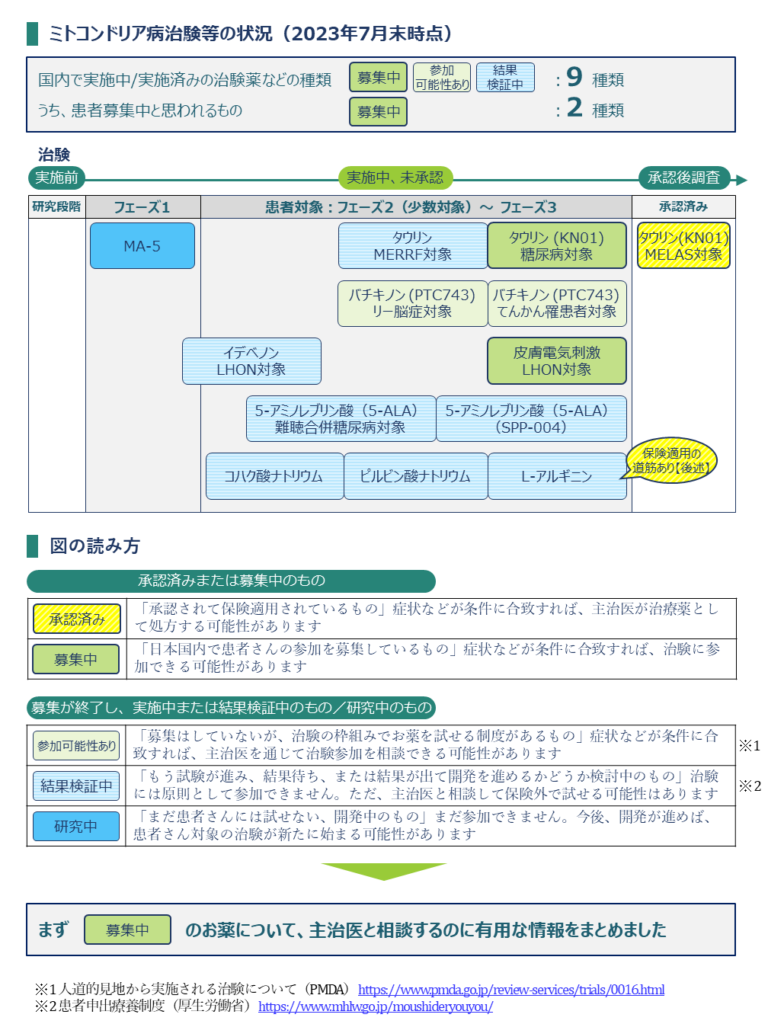
国内ミトコンドリア病治験等一覧(2023年7月末時点)
| No | 略称 | 承認の有無 | 進捗状況 | 備考 |
|---|---|---|---|---|
| 1 | タウリン(KN01) | 承認済 | 承認済み | MELASが対象 |
| タウリン(KN01) | 未承認、第II/III相 | 参加者募集中 | ミトコンドリア糖尿病(A3243G)が対象 | |
| タウリン(医師主導治験KN01とは別個) | 未承認、第II相? | 試験終了 | MERRFが対象 | |
| 2 | バチキノン(PTC743) | 未承認、第III相 | 参加者募集終了、試験継続中 | 難治性てんかんを伴うミトコンドリア病が対象 |
| バチキノン(PTC743) | 未承認、第III相 | 参加者募集終了、試験継続中 | リー脳症が対象 | |
| 3 | 皮膚電気刺激 | 未承認、第III相 | 参加者募集中 | レーベル遺伝性視神経症(11778)が対象 |
| 4 | 5-アミノレブリン酸/クエン酸第一鉄ナトリウム(5-ALA/SFC)(SPP-004) | 未承認、第III相 | 参加者募集終了、試験継続中 | 脳神経症状を中心とするミトコンドリア病が対象 |
| 5-アミノレブリン酸/クエン酸第一鉄ナトリウム(5-ALA/SFC) | 未承認、第II相? | 参加者募集終了、試験継続中 | 感音性難聴を合併するミトコンドリア糖尿病が対象 | |
| 5 | ピルビン酸ナトリウム | 未承認、第III相 | 試験中止 | リー脳症が対象 |
| 未承認、第III相 | 試験中止 | MELAS/MELAが対象 | ||
| 6 | L-アルギニン | 未承認、第III相 | 試験終了 | 寛解期MELAS(A3243G)が対象 |
| 未承認、第III相 | 試験終了 | 急性期MELAS(A3243G)(脳卒中様発作が発現してから6時間以内)が対象 | ||
| 7 | イデベノン | 未承認、第I/II相 | 試験終了 | レーベル遺伝性視神経症(11778)が対象 |
| 8 | コハク酸ナトリウム | 未承認、第II/III相 | 試験終了 | 女児1例への実施のみ |
| 9 | MA-5 | 未承認、第I相 | 研究中 |
ミトコンドリア病治験等の状況(2023年7月末時点)
国外で治験等進行中の医薬品候補について
| No | 開発企業・機関 | 医薬品候補 | フェーズ | 対象疾患 | 治験等対象国・地域 |
|---|---|---|---|---|---|
| 1 | PTC Therapeutics(米国) | Vatiquinone (PTC743/EPI-743):バチキノン | 2/3 | てんかんを伴うミトコンドリア病、20歳まで | 米国、フランス、イタリア、ポーランド、スペイン、スウェーデン、英国、カナダ、日本 |
| 3 | ミトコンドリア 病、過去の治験参 加者への継続投与 | 米国、イタリア、スペイン、英国 | |||
| https://www.ptcbio.com/our-pipeline/portfolio-pipeline/ | |||||
| 2 | Santhera Pharmaceuticals(スイス)、Chiesi Group(イタリア) | Idebenone:イデベノン | 4 ※EU承認済、市販後調査 | レーベル遺伝性視神経症(LHON)、12歳以上 | オーストリア、ベルギー、ブルガリア、ドイツ、イタリア、ポーランド、ポルトガル、スペイン、英国、米国 |
| https://chiesirarediseases.com/pipeline | |||||
| 3 | Stealth BioTherapeutics Inc.(米国) | Elamipretide:エラミプレチド | 3 | 核DNA変異に起因する原発性ミトコンドリア病、18~70歳 | 米国、デンマーク、フィンランド、ドイツ、ハンガリー、イタリア、オランダ、ノルウェー、スペイン、英国、オーストラリア、ニュージーランド |
| https://www.stealthbt.com/programs-pipeline/ | |||||
| 4 | GenSight Biologics(フランス) | GS010 (lenadogene nolparvovec) gene therapy:遺伝子治療薬GS010 | 3 | レーベル遺伝性視神経症(LHON)、発症1年以内、15歳以上 | フランス、ベルギー、イタリア、オランダ、スペイン、英国、米国、台湾 |
| https://www.gensight-biologics.com/diseases-we-target/ | |||||
| 5 | Zogenix, Inc.(米国)、UCB Biopharma SRL (ベルギー) | MT1621(デオキシヌクレオシドdC/dT) | 3 | チミジンキナーゼ2欠損症(TK2d)、18歳まで | 米国 |
| https://www.ucbjapan.com/Ourscience | |||||
| ※いったん実施を取り下げた模様 | |||||
| https://clinicaltrials.gov/ct2/show/NCT04581733 | |||||
| 6 | Reneo Pharmaceuticals Ltd(英国) | Mavodelpar (REN001): マボデルパル ※PPARδ 作動薬 | 2/3 | 原発性ミトコンドリアミオパチー、18歳以上 | 英国、ベルギー、チェコ、デンマーク、フランス、ドイツ、ハンガリー、イタリア、オランダ、ノルウェー、スペイン、米国、カナダ、オーストラリア、ニュージーランド |
| https://reneopharma.com/programs/ | |||||
| 7 | Astellas Pharma Inc.(米国) | Bocidelpar (ASP0367/MA-0211):ボシデルパル | 2/3 | 原発性ミトコンドリアミオパチー、18~80歳 | 米国 |
| https://www.astellas.com/jp/news/22901 | |||||
| https://ja.clinicaltrials.astellas.com/study/0367-CL-1201/ | |||||
| 8 | Khondrion BV(オランダ) | Sonlicromanol (KH176):ソンリクロマノール | 2 ※2023年内に進展見込 | A3243G変異を有するミトコンドリア病、18歳以上 | オランダ、デンマーク、ドイツ、英国 |
| 2 | 運動症状のあるミトコンドリア病、17歳まで | オランダ | |||
| https://www.khondrion.com/our-focus/ | |||||
| https://www.khondrion.com/2022-a-year-in-review/ | |||||
| 9 | Cyclerion Therapeutics(米国) | CY6463/IW-6463 ※可溶性グアニル酸シクラーゼ刺激薬 | 2 ※2023年内に進展見込 | MELAS、18歳以上 | 米国 |
| https://www.cyclerion.com/cy6463-melas/ | |||||
| ※被験者登録不調のため中止した模様(詳細不明) | |||||
| 10 | Abliva AB(スウェーデン) | KL1333(β-ラパコン誘導体) | 2 | ミトコンドリア病、18歳以上 | 英国、ベルギー、デンマーク、フランス、スペイン、米国 |
| https://abliva.com/research-and-development/ | |||||
| 11 | Omeicos Therapeutics GmbH(ドイツ) | OMT-28(オメガ3脂肪酸代謝物アナログ) | 2 | 原発性ミトコンドリア病、18~60歳 | ドイツ、イタリア |
| https://omeicos.com/pipeline/ | |||||
| 12 | Minovia Therapeutics, Ltd.(英国) | Mitochondrial Augmentation Therapy (MAT):ミトコンドリア増強療法 | 1/2 | ピアソン症候群、3~18歳 | イスラエル |
| 1 | 原発性ミトコンドリア病、4~18歳 | イスラエル | |||
| https://minoviatx.com/therapy/ | |||||
| 13 | Neurophth 纽福斯(中国) | NR082 (NFS-01), rAAV2-ND4 gene therapy:遺伝子治療薬NR082 (NFS-01) | 2/3 | レーベル遺伝性視神経症(LHON)、12~75歳 | 中国 |
| 1/2準備中 | G11778A変異を伴うレーベル遺伝性視神経症(LHON)、18~75歳 | 不明(おそらく米国) | |||
| NFS-02, rAAV2-ND1 gene therapy:遺伝子治療薬NFS-02 | 不明 | G3460AほかND1に点変異を伴うレーベル遺伝性視神経症(LHON) | 中国 | ||
| 1/2準備中 | G3460A変異を伴うレーベル遺伝性視神経症(LHON)、18~75歳 | 不明(おそらく米国) | |||
| https://www.neurophth.com/en/ProjectD-65.html | |||||

【解説】治験等に参加するには(※募集中でない「参加可能性あり」の治験を含む)
患者から相談を受けた主治医が、患者の意思を確認した上で、治験を実施する担当窓口へ治験参加を打診します。(窓口は主に企業ですが、医師が主導する治験では医療機関の場合もあります。) 主治医は、治験実施医療機関の医師とともに、患者が治験に参加できるか、医学的見地から検討します。
【医学的見地からの検討結果】主に3通りの流れがあります
● 既存の治療を継続することが最善、と判断されます(治験には参加しません)。
● 治験に参加できる可能性がある、と判断され、被験者としての参加へ進みます。
●【特例的な扱い(※1)】そのままでは治験に参加できないものの、主治医が治験実施企業に対して、治験と同じ枠組みを新たに設定して同じ治験薬を提供してもらうよう要望できます。(ただ、治験には本来の目的があるため、開発に支障が出るなどの理由で企業側が断ることもあります。実現する場合も、検討に時間を要したり、一部費用が患者負担になったりすることがあります。)
● 治験に参加できる可能性がある、と判断され、被験者としての参加へ進みます。
●【特例的な扱い(※1)】そのままでは治験に参加できないものの、主治医が治験実施企業に対して、治験と同じ枠組みを新たに設定して同じ治験薬を提供してもらうよう要望できます。(ただ、治験には本来の目的があるため、開発に支障が出るなどの理由で企業側が断ることもあります。実現する場合も、検討に時間を要したり、一部費用が患者負担になったりすることがあります。)
【ご注意】治験をはじめとする研究段階の医療は制度が複雑なため、このレポートでは大胆に簡略化しました。ジーネックスは主治医の先生がお探しの情報も可能な限り提供しますので、必要に応じて直接お問い合わせいただくようお伝えください。 このページは、公開されている臨床試験情報を分かりやすくお伝えする趣旨でジーネックスが独自に作成したものであり、個別の治験への被験者募集を目的とする情報提供ではありません。